Wieso zieht Valneva seine Standardzulassung zurück?
Update 17. Nov. 10:00 Uhr: Kurzgutachten zum Valneva Impfstoff von Dr. Hans-Joachim Kremer (deutscher Apotheker) vom 25. Oktober 2023
Nebenwirkungen: Solicited adverse reactions
Dr. Hans-Joachim Kremer
FAZIT: Die Inzidenz von mutmaßlichen Nebenwirkungen spricht, angesichts des
minimalen Wirksamkeit und des höchstwahrscheinlich nicht vorhandenen Nutzens klar
gegen diese Impfstoffe, also sowohl gegen Vaxzevria als auch gegen Valneva. In meinen
Augen sind beide Produkte Paradebeispiele für einen schlechten Handel („bad deal“).
Sicherheit: Unerwünschte Ereignisse
FAZIT: Die Sicherheit ist derzeit auf Basis der Studiendaten kaum zu bewerten.
Schwere Verläufe
FAZIT: Der Effekt von Valneva auf schwere Verläufe wurde nicht nachgewiesen. AlleDaten zeigen in die Richtung, dass kein klinisch-relevanter Effekt vorliegt.Beim Vaxzevria selbst verbleiben in dieser Hinsicht Fragezeichen. Unterm Strich kannjedenfalls auch hier nicht von einem klinisch-relevanten Effekt gesprochen werden.
Wer ist Dr. Hans-Joachim Kremer?
Als deutscher Apotheker mit Promotion im Bereich Pharmakologie, dem Europäischen Zertifikat für Pharmazeutische Medizin und dem entsprechenden Schweizer Diplom blicke ich auf einen Erfahrungsschatz aus der internationalen klinischen Forschung und Entwicklung von Arzneimitteln seit 1988 und aus der Pharmabranche allgemein seit 1980 zurück. Abschnitte meiner Industriekarriere waren Sandoz Pharma AG in Basel, Schweiz, das Auftragsforschungsinstitut Focus in Neuss und ASTA Medica / VIATRIS in Frankfurt.
Beitrag
Update 17:00 Uhr am Ende des Beitrags
Der Impfstoff des französischen Biotechnologieunternehmens Valneva wurde nach dem Firmennamen Valneva (VLA2001) benannt und bekam seine Standardzulassung am 24. Juni 2022. Nun soll mit der Gabe aber Schluss sein, dass Unternehmen widerruft die Zulassung. Ist aber nicht weiter tragisch, steht doch schon der nächste Impfstoff von Valneva in den Startlöchern. Dank der FDA-Zulassung gibt es nun den IXCHIQ-Impfstoff. Der erste Chikungunya-Impfstoff für die Altersgruppe zwischen 12 und 18 Jahren.
Valneva SE ist ein französisches Biotechnologieunternehmen mit Sitz in Saint-Herblain in Frankreich. Es entwickelt und vermarktet Impfstoffe gegen Infektionskrankheiten und hat Produktionsstätten in Livingston, Schottland, Solna, Schweden, und Wien, Österreich.
COVID-19-Impfstoff (inaktiviert, adjuvantiert) Valneva ist angezeigt für die aktive Immunisierung zur Vorbeugung gegen durch SARS-CoV-2 hervorgerufenes COVID-19 bei Personen zwischen 18 und 50 Jahren
EMA
Bei der Aktionär heißt es zu den Umsätzen des Unternehmens:
Mit IXCHIQ gegen das Chikungunya-Virus hat Valneva nun den dritten Reiseimpfstoff zur Zulassung geführt. Die Vakzine IXIARO und DUKORAL sorgen bereits für Umsätze. Dank der Erholung im Reise-Business konnte Valneva in den ersten neun Monaten des Jahres die Produkterlöse um knackige 42,6 Prozent auf 106,1 Millionen Euro steigern.
Für das Gesamtjahr 2023 peilt das Management rund um CEO Thomas Lingelbach Produktumsätze zwischen 130 und 150 Millionen Euro an. Für Forschung und Entwicklung will das Unternehmen im laufenden Kalenderjahr insgesamt 60 bis 70 Millionen Euro in die Hand nehmen.
13.11.2023
Der neue Impfstoff befindet sich laut Valneva aktuell noch im Prüfverfahren. Ob die Zulassungsstudien auch so aussehen wie die für den Corona-Impfstoff?
Zulassungsstudie von Valnevafür das Covid-Vakzin
Da uns die Zulassungsstudie interessiert hat, haben wir mal kurz im „www“ gestöbert und stießen auf den „ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS“ der EMA. In der Studie wurde der Valneva Impfstoff (VLA2001) mit dem Vektorimpfstoff von AstraZeneca (ChAdOx1-S) beurteilt. Dies nennt sich wohl Immunobridging-Studie. Wie man auf die Idee kommt, in einer Zulassungsstudie den eigenen Impfstoff mit einem anderen neu und ziemlich zügig auf den Markt geworfenen Impfstoff vergleichen zu wollen, ist zumindest für uns nicht ganz plausibel. Zumal man bei AstraZeneca bereits im März 2021 die ganzen Vorfälle wegen Blutgerinnseln hatte. Hat man eigentlich zu den Ergebnissen aus dieser Studie je etwas in Bezug auf den AstraZeneca Impfstoff gehört? Das ist uns zumindest nicht bekannt.
Gerade einmal 2.975 Menschen wurden in der Studie damit gespritzt, 1.978 erhielten Valneva und 997 den AstraZeneca Impfstoff. Darüber hinaus erhielten in einer weiteren Behandlungsgruppe 1.042 ebenfalls den Valneva Impfstoff. Wieso die Gruppen nicht gleich groß gewählt wurden, ist aus dem Dokument der EMA nicht ersichtlich.
Primäre Impfserie
Die Immunogenität von COVID-19-Impfstoff Valneva als primäre Impfserie wurde in einer im Vereinigten Königreich durchgeführten randomisierten, beobachterverblindeten, aktiv kontrollierten Studie der Phase III zur Sicherheit und Immunogenität (VLA2001-301) beurteilt. Die Studie verglich
VLA2001 mit einem zugelassenen Covid-19-Vektorimpfstoff (ChAdOx1-S [rekombinant]) bei Erwachsenen, wobei auch Personen mit stabiler Erkrankung eingeschlossen waren. Insgesamt wurden 2.975 Teilnehmer im Alter von ≥ 30 Jahren im Verhältnis 2:1 randomisiert und einer 2-Dosen-Impfserie mit VLA2001 (n = 1.978) oder COVID-19-Impfstoff (ChAdOx1-S [rekombinant]) (n = 997), verabreicht jeweils im Abstand von 28 Tagen, zugewiesen. Zudem wurden 1.042
Teilnehmer im Alter von 18 – 29 Jahren in eine nicht randomisierte Behandlungsgruppe aufgenommen und erhielten VLA2001 offen.
Beruhigend zu wissen, dass anhand der bislang vorliegenden Daten „zur Toxizität bei wiederholter Gabe und
zur Reproduktions- und Entwicklungstoxizität” sich „keine besonderen Gefahren für den Menschen erkennen“ lassen. Das scheint richtig zu sein, aber anhand von Daten zu 1.978 und 1.042 Studienteilnehmern eine Standardzulassung zu erhalten, zeigt, dass Sicherheit sicherlich nicht der wichtigste Aspekt war. (außer wir haben natürlich eine weitere Studie übersehen, welche zur Zulassung führte)
Genotoxizität/Karzinogenität
Es wurden keine Studien zur Genotoxizität oder Karzinogenität durchgeführt. Es wird nicht davon ausgegangen, dass die Bestandteile des Impfstoffs genotoxisches Potenzial aufweisen.
Reproduktionstoxizität
Eine Studie zur Reproduktionstoxizität, in der VLA2001 bei weiblichen Han Wistar-Ratten untersucht wurde, zeigte, dass VLA2001 keine Auswirkungen auf die reproduktiven Parameter, die Geburt oder die Entwicklung der Föten hatte. Es liegen keine Daten zur Plazentagängigkeit des Impfstoffs oder dem Übergang in die Milch vor.
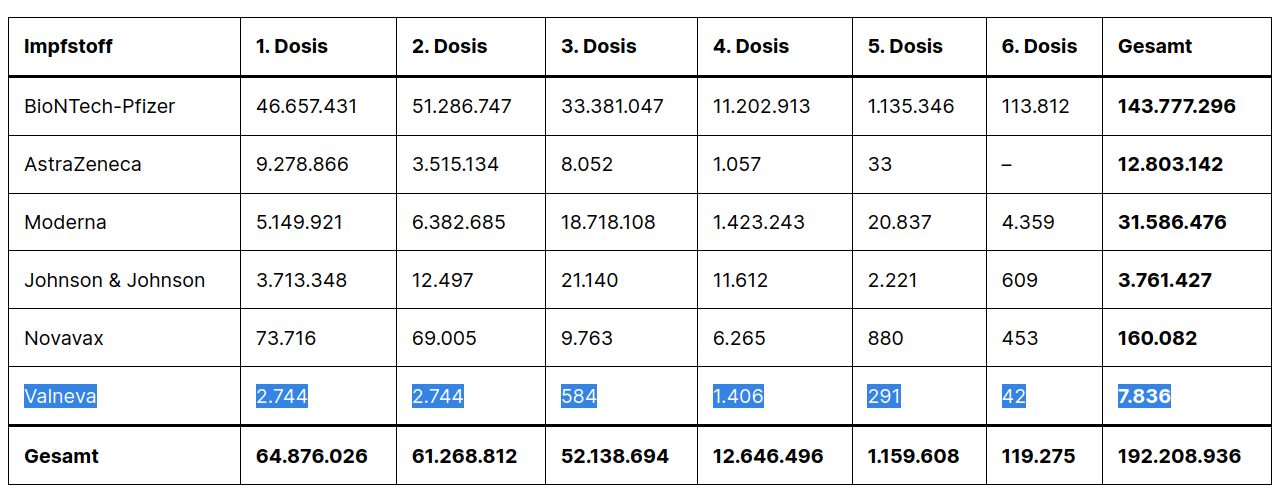
7.836 Dosen wurden von Valneva in Deutschland verimpft
Im 21. PEI Sicherheitsbericht ist die Rede davon, dass insgesamt 7.836 Dosen in den Armen der Deutschen gelandet sind. Es gab 4 Verdachtsfallmeldungen zu Impfnebenwirkungen im 21. PEI Sicherheitsbericht. Im 20. PEI Sicherheitsbericht gab es demnach dann noch keine Meldungen. Formulieren wir es besser mal so zumindest wurde dies nicht erwähnt.
Die EMA weist allerdings doch auf ein paar wenige leichte Nebenwirkungen im „ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS“ hin. In der „Tabelle 1. Nebenwirkungen aus Schlüsselstudien“ werden dann doch ein paar Nebenwirkungen genannt, welche die „üblichen“ übersteigen. Konkrete zahlen erfährt man nicht, lediglich eine Häufung. Beispielsweise können „Oropharyngeale Schmerzen“ auftreten, was den Mund- und Rachenraum betrifft. Gelegentlich treten auch „Arthralgien“ auf, welches die Schmerzhaftigkeit eines Gelenkes bezeichnet. Auch Muskelkrämpfe sollen die Menschen gehabt haben und ebenfalls eine „Lymphadenopathie“ (Lymphknotenschwellung). Zum Glück trat nur selten eine „Thrombozytopenie“ auf, zumindest wenn man den Unterlagen Glauben schenken mag. Trat die bei den AstraZeneca Geimpften auf oder auch bei den Valneva Probanden?
Dass es bei Studien allerdings nicht unbedingt immer mit rechten Dingen zu geht, vor allem weil die Pharmakonzerne diese selbst durchführen und beeinflussen können, zeigt sich zumindest für uns.

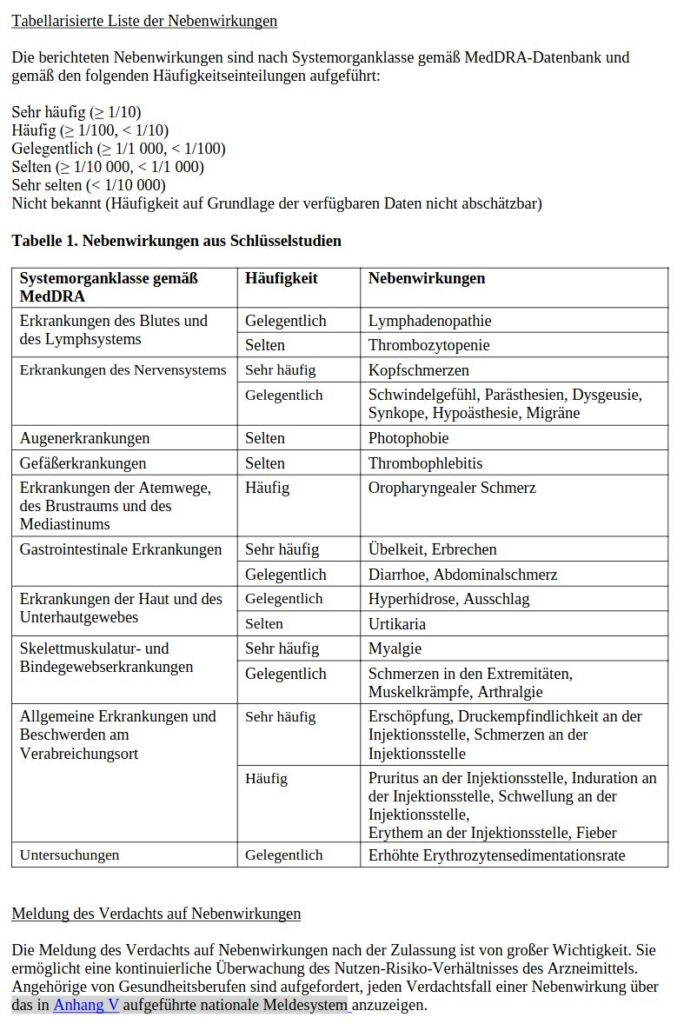
Am Ende der Tabelle darf natürlich die Standardfloskel nicht fehlen. Die Meldung des Verdachts auf Nebenwirkungen ist von großer Wichtigkeit. Aber nur so lange niemand etwas meldet und selbst dann bleiben wir einfach bei der Begrifflichkeit Verdachtsfall.
Jetzt ist aber Schluss – Widerruf der Zulassung zum 30. November 2023
Zum 30. November wird also die Zulassung widerrufen. Aber alle können aufatmen, es gibt durch den Bund ja weiterhin bereitgestellte Alternativen. Wieso diese Zulassung widerrufen wird, haben zumindest wir nicht erfahren.
Valneva COVID-19-Impfstoff – Ende der Haltbarkeitsdauer und Widerruf der Zulassung zum 30. November 2023
Im Zentrallager des Bundes erreichen sämtliche Chargen des COVID-19 Impfstoffs des pharmazeutischen Unternehmers Valneva das Ende der Haltbarkeitsdauer. Die Zulassung wird außerdem auf Antrag des pharmazeutischen Unternehmers zum 1. Dezember 2023 widerrufen.
Eine Verwendung nach dem 30.November 2023 ist daher unzulässig.
Sofern der Impfstoff noch in Arztpraxen lagert, ist dieser mit Ablauf des Monats November fachgerecht zu entsorgen. Als Alternative stellt der Bund weiterhin COVID-19 Impfstoffe der pharmazeutischen Unternehmer BioNTech, Moderna (ausgenommen Spikevax XBB.1.5) und künftig Novavax bereit.
Rundschreiben der Kassenärztlichen Vereinigung Niedersachsen
An der Haltbarkeit alleine kann es wohl nicht liegen, hätte man dies doch durch das PEI einfach in die Wege leiten können. Schließlich wurde die ja schon mal durch die EMA am 17.02.2023 verlängert.

Auch Soldaten wurden mit Valneva geimpft
Am 25. Oktober wird in der Telegram Gruppe „Keine Covidimpfung für Soldaten“ auf ein Gutachten zum Valneva Impfstoff hingewiesen. Dieses wohl bei 2 noch laufenden Wehrbeschwerdeverfahren beim BVerwG eingebracht werden soll.
Ein absoluter Experte (Apotheker mit Promotion und viel Erfahrung im Bereich der Pharmakologie) hat zu dem Totimpfstoff VALNEVA ein sehr gutes Gutachten verfasst. Dieses Gutachten wird RA Wilfried Schmitz in 2 noch laufenden (!) Wehrbeschwerdeverfahren beim BVerwG einbringen. Den Spendern, die zugesagt haben, dass sie sich an den Kosten für dieses Gutachten beteiligt werden, wird dieses Gutachtn zum Dank per Mail als PDF übermittelt werden. Im Namen der beiden Beschwerdeführer bedanken wir uns ganz herzlich bei den Spendern. Aus unserer Sicht hat sich jedenfalls gezeigt, dass VALNEVA keine (!) akzeptable Ausweichoption ist.
Pressemitteilung von Valneva zur Standardzulassung
Was sind die Hintergründe?
Auch RAin Brigitte Röhrig äußert sich in ihrem Telegram Kanal heute zu dieser Thematik recht ausführlich. Die Anwältin vermutet wirtschaftliche Gründe für den Widerruf der Standardzulassung von Valneva.
Aller Wahrscheinlichkeit werden dem Widerruf der Zulassung wirtschaftliche Gründe zugrunde liegen.
RAin Röhrig
KBV meldet, dass VALNEVA die Zulassung für seinen COVID-Impfstoff zum 1.12.2023 widerruft
Bisher keine Information darüber auf PEI und EMA-WebseiteWie aus obigem Post ersichtlich, informiert die KBV darüber, dass der COVID-Impfstoff von Valneva ab dem 1. Dezember 2023 nicht mehr verfügbar sei. Die Haltbarkeit laufe am 30. November ab und das Unternehmen habe zum 1.12.2023 die Zulassung widerrufen.
Interessanter Weise finden sich derzeit weder auf der EMA-Webseite zum Produkt noch auf der Webseite des PEI zu dem Produkt entsprechende Informationen – und das, obwohl die KBV angibt, diese Information vom ZEPAI (Zentrum für Pandemieimpfstoffe und -Therapeutika) beim PEI erhalten zu haben.
Jetzt wird spekuliert, warum Valneva die Zulassung widerruft bzw. auf sie verzichtet. Was können die Gründe sein?
Beantragt ein Zulassungsinhaber den Widerruf seiner Zulassung bzw. verzichtet er auf die Zulassung, hat er dies der EU-Kommission einschließlich seiner Gründe für diese Entscheidung mitzuteilen, Art. 13 (4) Unterabsatz (UA) 2, 14b der VO 726/2004/EG. Diese Meldung sollte grundsätzlich spätestens 2 Monate vor der Beendigung des Inverkehrbringens erfolgen (Art. 13 (4) UA 2).
Grundsätzlich kann ein Widerruf der Zulassung durch den Zulassungsinhaber auf einem geänderten Nutzen-Risiko-Profil, der Erkenntnis der Schädlichkeit oder anderen Problemen mit der Sicherheit und / oder Wirksamkeit basieren. In diesen Fällen wäre der Zulassungsinhaber verpflichtet, eine entsprechende Initiative zu starten und die EMA zu informieren bzw. von sich aus den Widerruf zu erklären, Art. 107 ff des Gemeinschaftskodex (RL 2001/83/EG).
Aus dem letzten Beurteilungsbericht zum PSUR aus September 2023 für den Zeitraum vom 28. August 2022 bis 27. Februar 2023 ergibt sich, dass auf Basis des PSUR der zuständige Pharmakovigilanz-Ausschuss der EMA aufgrund unveränderten Nutzen-Risiko-Profils die Aufrechterhaltung der Zulassung befürwortete.
Im Hinblick auf die von Valneva angegebenen Daten zu ausgelieferten und verimpften Dosen gab es seitens des Ausschusses ausdrücklich festgestellte Unklarheiten:
Valneva wurde aufgefordert, im nächsten PSUR diese Daten für den Zeitraum seit der Zulassung so klar wie möglich darzustellen (S. 8). Die Disproportion zwischen ausgelieferten und verimpften Dosen sei wesentlich.
Wenn die Daten nur annähernd stimmen sollten, dann wäre die Verabreichung des Valneva COVID-Impfstoffes ein großer Misserfolg:
Alleine in Deutschland stünden 751.200 ausgelieferten Dosen lediglich 7.087 verimpften Dosen gegenüber.
Deutschland hätte Valneva bis zum 27.2.2023 744.000 Impfdosen abgekauft, ohne dass entsprechende Nachfrage bestand.
Auch hier zeigt sich wieder eine dramatische Fehlkalkulation zu Lasten des deutschen Steuerzahlers
Aller Wahrscheinlichkeit werden dem Widerruf der Zulassung wirtschaftliche Gründe zugrunde liegen.
News: Tagesaktuelle Artikel von Lesern für Leser – diese Seite dient dazu, dass ihr euch im Kommentarbereich über aktuelle wichtige News und Nachrichten informieren und austauschen könnt.
8 Antworten auf „Wieso widerruft Valneva die Standardzulassung seines Covid-Vakzins – verabreicht an 2.744 Menschen“
Bedeutet „beobachterverblindet“ / „observer blinded“ wieder das gleiche wie bei Bioncash-Comirnaty, nämlich, dass wir, die Beobachter blind sind, während bei der Studie die Patienten, Ärzte und Gutachter alle über die Gruppenzuordnung bescheid wissen? Scheint mir das neue Tarnwort von Big Pharma zu sein.
Der Vergleich mit einem echten Placebo ist der Härtetest für jedes Medikament, der sofort die Nutzlosigkeit und Gefährlichkeit vieler Medikamente offen legen würde. Deswegen hat Big Pharma über die Jahre einen bunten Strauß von weichgespülten Alternativen und ebenso vielen Ausreden entwickelt, um den echten Placebo-Vergleich nicht durchführen zu müssen. Entweder wird mit dem gleichen Medikament in geringerer Dosis verglichen oder mit einem bekannten Konkurrenzprodukt oder mit einem Scheinplacebo. Scheinplacebos sind bei Impfstoffen sehr beliebt. Ein Scheinplacebo ist eben keine Kochsalzlösung, sondern an sich der vollständige Impfstoff, ausgenommen das, was Virologen als Viren bezeichnen. Aber ansonsten sind alle „Wirkverstärker“ (Quecksilber- oder Aluminiumverbindungen) und Konservierungsstoffe enthalten. Die Ausrede dafür lautet: Es wäre unethisch, den Patienten in der Kontrollgruppe den Wirkstoff vorzuenthalten.
Offensichtlich ist das ein Zirkelschluss, denn die Wirksamkeit soll mit dem Placebovergleich ja erst nachgewiesen werden. Aber Entscheider und Ärzte und Patienten haben es in der Regel nicht so mit Logik und sind mit dieser Schummelei einverstanden.
Aus der Presseerklärung von Valneva vom 9.11.23:
INAKTIVIERTER SARS-CoV-2 GANZVIRUS-IMPFSTOFF
Valnevas COVID-19 Impfstoff VLA2001 ist der einzige inaktivierte COVID-19 Ganzvirusimpfstoff, der in Europa[36] und war der erste COVID-19-Impfstoff, der von der EMA eine vollständige Marktzulassung erhielt.
Angesichts des geringeren Auftragsvolumens im Zusammenhang mit dem Rückgang der COVID-19-Pandemie hat Valneva die Herstellung des Impfstoffs im August 2022 eingestellt und die Vorräte zum 31. Dezember 2022 vollständig abgeschrieben. Um zusätzliche Kosten im Zusammenhang mit dem Impfstoff, einschließlich Lizenzgebühren, einzusparen, hat Valneva vor kurzem den Rücktritt der Zulassung von VLA2001 in Europa beantragt. Der Rücktritt wurde von der EMA akzeptiert und wird am 1. Dezember 2023 wirksam.
In den ersten neun Monaten des Jahres 2023 belief sich der Umsatz von VLA2001 auf € 5,7 Mio. verglichen mit € 23,9 Mio. in den ersten neun Monaten des Jahres 2022.
https://valneva.com/press-release/valneva-reports-nine-month-2023-financial-results-and-provides-corporate-updates/?lang=de
Noch ein interessanter Artikel vom 8.12.22.
https://www.lesechos.fr/industrie-services/pharmacie-sante/covid-le-vaccin-de-valneva-obtient-un-avis-defavorable-des-autorites-sanitaires-1887171
Die französische Gesundheitsbehörde (Haute Autorité de Santé HAS) hat im Dezember 2022 von der Verwendung des Valneva-Impfstoffes abgeraten. Es gäbe nicht genügend Daten über die Wirksamkeit; im übrigen gäbe es genügend andere Impfstoffe für diejenigen, die keine mRNA-Stoffe wünschten. (Seltsamerweise wird in dem Zusammenhang auch Moderna empfohlen.) Für Booster-Impfungen empfiehlt die HAS in erster Linie Pfizer, ggf. auch Novavax.
Dazu bei tkp:
https://tkp.at/2023/11/17/valneva-der-wundersame-covid-19-impfstoff/
Zitat:
„Beim Valneva soll es sich um einen gereinigten, inaktivierten und adjuvantierten Ganzvirus-Impfstoff gegen SARS-CoV-2 (Wuhan-Stamm hCoV-19/Italy/INMI1-isl/2020, der in Vero-Zellen gezüchtet wurde) handeln; mithin keine Gentechnik, dafür ähnlich den etablierten Grippe-Impfstoffen.
Es ist verwunderlich, dass die Hersteller von Valneva sich nie um die 1,5 Millionen € bewarben, die von der Gruppe Next Level (um Dr. Stefan Lanka, Isolate Truth Fund) für die Isolierung des SARS-CoV-2 Virus und anschließenden Nachweis der Koch’schen Postulate ausgelobt wurden. Wo Sie doch angeblich den Wuhan-Virus anzüchten und vermehren konnten und das Geld, mangels Umsätzen, sicher bestens hätten gebrauchen könnten.“
Ja, so geht das nunmal im Kapitalismus. Da werden Produzenten ganz einfach gekauft. Also bspw. dafür bezahlt daß sie bestimmte Produkte eben nicht produzieren oder Lizenzen an Andere abtreten.
Was für eine Überraschung!
Machen Sie das extra mit dem Wort „Kapitalismus“ hier nun wieder zwei, drei Kommentatoren zu triggern, die dann wieder die gleichen Romane hier verfassen wie schon hundert Male gelesen?
Viel über den Blogbeitrag wissen Sie ja nicht zu sagen. Aber den Blogbetreiber wieder in „Schwerstarbeit“ deshalb zu versetzen, weil Sie mit „Kapitalismus“ mal wieder etliche triggern, und dann „reden“ Sie fleißig „mit“…
Ihr Kommentar hier ist ja kein Einzelfall, denn Sie geben sich heute wieder echt Mühe… https://corona-blog.net/2023/11/16/impfarzt-axel-linz-ist-kein-unverantwortlicher-querdenker-sieht-covid-impfung-jetzt-aber-als-zeitbombe/#comment-94157
Ach Leute, das hat doch mit der Wirksamkeit nichts zu tun. Werden die Impfstoffe der Anderen etwa zugelassen weil sie wirksamer sind!? MFG
Es etwas faul im Staate Dänemark. Die Zulassungsstelle sieht durch den Widerruf von Valneva jetzt ziemlich düpiert aus. Das entbehrt nicht einer gewissen Komik.